mol ist die Bezeichnung für eine Zahl, nämlich die Anzahl der Kohlenstoffatome in 12 g reinen Kohlenstoff. In diesen 12 g Kohlenstoff sind laut Loschmidt 6,023 * 10 hoch 23 Kohlenstoffatome enthalten. Das ist zwar eine ziemlich große Zahl, aber eine abzählbare und damit vor allem eine natürliche Zahl, trotz der Potenzschreibweise! Bei der Angabe „6,023 * 10 hoch 23“ fehlen nämlich 20 Stellen. In der Dezimalschreibweise würde diese Zahl so aussehen:
602.3xx.xxx.xxx.xxx.xxx.xxx.xxx oder 602 Trilliarden 3xx Trillionen … (hoffentlich hat sich der Herr Loschmidt da nirgendwo verzählt 🙂 aber es sind ja sowieso 20 Stellen unbekannt)
Analogien
Die Zahl 3,141… bezeichnen wird mit einem griechischen Buchstaben π (pi).
Die Zahl 1 bezeichnen wir mit dem Wort eins.
Die Zahl 0,01 (oder 1/100) bezeichnen wir mit 1 Prozent oder dem Symbol 1 %.
Die Zahl 0,001 (oder 1/1000) bezeichnen wir mit Promill oder dem Symbol 1 ‰.
Also können wir die Zahl 6,023 * 10 hoch 23 auch mit mol bezeichnen. Die Multiplikation mit 1 (wie bei 1 mol) ändert nichts an der Zahl.
Achtung – Achtung
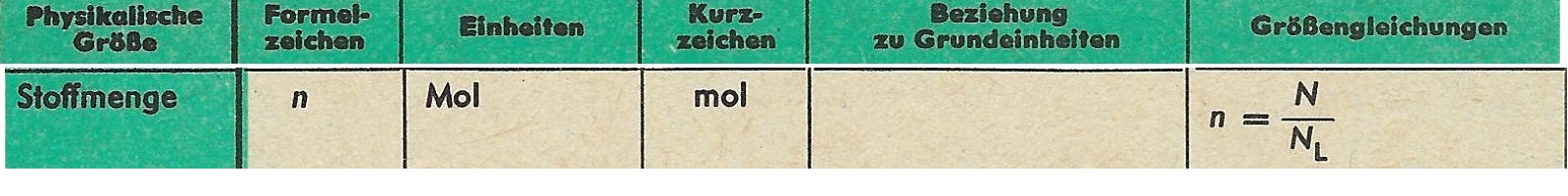
1 mol darf auf keinen Fall mit 1 Mol verwechselt werden. Bei ´1 mol´ handelt es sich um eine Zahl, bei ´1 Mol´ um die Menge eines beliebigen Stoffes, die 6,023 * 10 hoch 23 Einzelteile enthält (siehe auch den Artikel Stoffmenge im Lexoekon).
Die Gleichsetzung von Mol und mol (wie in den folgenden Tabellen) ist damit falsch und muß dringend korrigiert werden.